2025年,面对药品技术审查业务量持续攀升的新形势,在选派5名骨干赴国家局药审中心培训6个月的人手紧缺的情况下,省药品和医疗器械审评服务中心主动担当、精准发力、两线作战,通过优化流程、强化服务、升级能力,全力保障药品审查工作高效推进,以6个月培训考核优秀的成绩推动国家局优化药品补充申请审评审批程序改革试点获批,并保质高效完成了683件备案类变更技术核查和886个品种的再注册申请,同比分别增长36%和374%,有力支撑我省生物医药产业高质量发展。
一、提质增效办件,精准审评赋能
(一)药品备案类变更
全年完成药品备案类变更事项683件,同比增长36%。
按品种类别,全年办结化药制剂618件,中药制剂40件,原料药25件。
按申报事项类别,全年办结办件涉及11种申请事项类别,共有805个申报事项。排在前5名的申报事项共计707个,分别为变更有效期和贮藏条件、变更制剂生产工艺、变更制剂所用原料药的供应商、变更生产场地、变更生产批量,分别占已完成总数的31.2%、23.3%、15.0%、11.3%、6.8%。
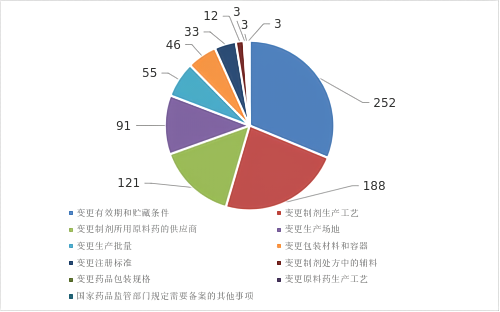
按制剂剂型,注射剂(注射液、注射用无菌粉末、注射用浓溶液)307件,占比45%;口服固体制剂(片剂、胶囊剂、颗粒剂)249件,占比36%;其余剂型127件,占比19%。
(二)药品再注册
全年完成药品再注册事项886件,同比增长373.8%。
按品种类别,全年办结化学制剂734个、中药制剂96个、原料药53个、生物制品3个。
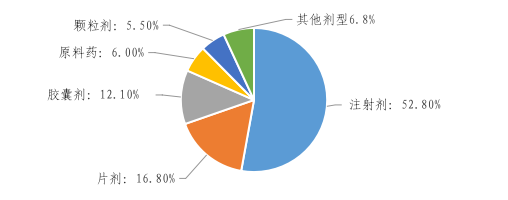
按制剂类型,涉及23种剂型,排在前5名的分别为注射剂、片剂、胶囊剂、原料药、颗粒剂,分别占已完成总数的52.8%、16.8%、12.1%、6.0%、5.5%。
二、深化审评改革,聚力产业发展
(一)完善分级分类审评新机制,提高审评效能
中心试行分级分类审评,对审评流程实施“四类分级、差异管理”,制定分类审评细则,合理分配审评资源,药品备案类变更、再注册技术审查平均用时较法定时限提速约27%、45%,全力构建适应产业发展与安全需求的新型审评体系。
(二)强化前置服务与沟通指导,保证资料质量
审评中心积极拓宽服务渠道,通过前置辅导、宣贯培训、共性问题解答、申报前沟通会议等形式,精准助力企业理解新规要求,2025年共发布药品共性问题13期,技术咨询148次;为我省两家企业申报4个1.1类中药提供了2次面对面技术指导,为1家医疗机构提供技术咨询,助力其申报的含海洋药材的医疗机构制剂成功备案。
(三)提升审评员风险研判能力,统一审查尺度
2025年,审评中心通过积极参加线上线下培训、聘请外部专家授课、选派业务骨干组成专项审评团队赴CDE跟班学习等方式,综合提升审评员风险研判能力,并定期通过内审和交叉复核的模式,持续加强审查尺度的统一。
版权所有:海南省药品和医疗器械审评服务中心
地址:海南省海口市南海大道53号
技术支持:海南信息岛技术服务中心
